医药专利案件中补交实验数据的问题是近年来专利界争议极大的一个问题。为了解决这一问题上的争议,最高人民法院于2018年6月1日对外发布的《关于审理专利授权确权行政案件若干问题的规定(一)(公开征求意见稿)》(以下简称征求意见稿)第十三条作出了规定:“化学发明专利申请人、专利权人在申请日以后提交实验数据,用于进一步证明说明书记载的技术效果已经被充分公开,且该技术效果是本领域技术人员在申请日根据说明书、附图以及公知常识能够确认的,人民法院一般应予审查。化学发明专利申请人、专利权人在申请日以后提交实验数据,用于证明专利申请或专利具有与对比文件不同的技术效果,且该技术效果是本领域技术人员在申请日从专利申请文件公开的内容可以直接、毫无疑义地确认的,人民法院一般应予审查。”
该条规定区分补交的实验数据的不同证明目的,采取了不同的标准,即在适用专利法第26条第3款和第22条第3款时对当事人补交的实验数据采取不同的司法审查标准。目前这只是一个征求意见稿,社会公众可以向最高法院提出意见和建议。本文借机尝试对这一问题进行深入的梳理,从专利法法理上进行分析,然后对最高法院的征求意见稿进行评价并提出修改建议。
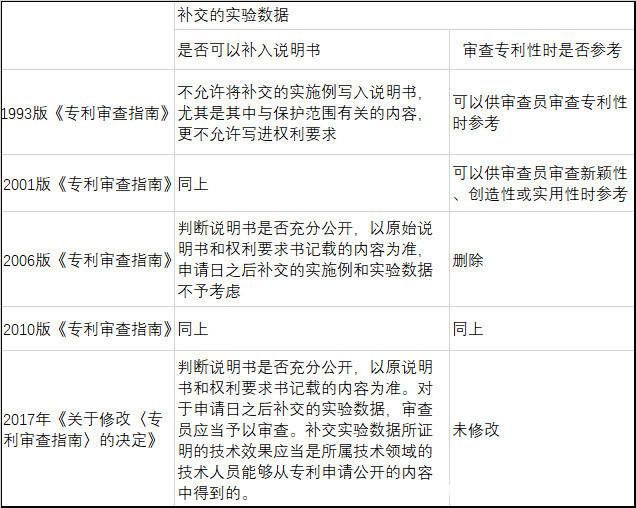
一、历次版本《专利审查指南》的有关规定
2017年《关于修改〈专利审查指南〉的决定》规定,对于申请日之后补交的用于证明说明书充分公开的实验数据,审查员应当予以审查。但同时又规定“补交实验数据所证明的技术效果应当是所属技术领域的技术人员能够从专利申请公开的内容中得到的。”何谓“得到”?是指直接得到,还是既包括直接得到也包括推导得到?见仁见智。
二、法院对补充实验数据的审查标准
关于当事人补交的实验数据,北京市高级人民法院知识产权庭2017年发布的《当前知识产权审判中需要注意的若干法律问题》明确了如下几点意见:第一,补充提交的实验数据所证明的技术效果在原专利申请文件中有明确的记载,并且其证明的事实不能超过原始申请文件公开的范围,不能用于证明新的技术事实;第二,无论权利人提交补充实验数据是用于克服说明书未充分公开,还是用于证明本专利具备创造性,该补充证据的采信标准是一致的;第三,补充实验数据的内容虽然规定在《专利审查指南》关于化学领域审查章节,也适用于其他技术领域;第四,该实验数据应当是采用专利申请日前的实验条件、设备和实验手段所获得的。
目前北京法院对待当事人补交的实验数据的审查标准是该实验数据系采用涉案专利申请日前的实验方法获得的,其所证明的技术效果在原专利申请说明书有明确记载。最高人民法院则由(2012)知行字第41号案中“不得引入新的技术内容和违反专利先申请原则”的严格标准趋于宽松。
三、域外的审查标准
欧美及亚洲的日本是专利大国、强国,其有关经验值得我们参考借鉴。关于如何对待当事人补交的实验数据,欧洲专利局2012年6月的《专利审查指南》规定:审查员在评价创造性时考虑的相关证据可以由申请人在随后的审查程序中提交,对任何时机提出的支持创造性的新效果的证据都应给予关注。只有隐含地存在于原始提交的申请文件或至少与原始提交的申请文件中的最初技术问题相关的新效果才会被考虑。[5]美国联邦巡回上诉法院认为,如果预料不到的技术效果可以从专利文件中公开的方法隐含得出,或者与公开产品的用途局域紧密的联系时,在后的实验证据应当被考虑。[6]日本法院认为,如果补交的实验数据是从原说明书公开的内容中可以认识到或者推导得出的,则该实验数据应当被接受。[7]综合起来看,欧洲、美国及日本均认为,只要补交的实验数据所证明的技术效果是原说明书中公开的、隐含的或者可以推导得出的,都应当予以考虑。这个标准与专利先申请原则是符合的,具有合理性,值得我们借鉴。与之相比,我国专利复审委员会以及法院的审查标准偏严。
四、对补交实验数据的审查标准的分析
对于补交的实验数据的审查,主要涉及专利法的以下原则:
第一,专利先申请原则。专利先申请原则是我国专利法上的一项基本原则,在是否采纳当事人补交的实验数据这一问题上,也应当遵守该原则。当前的专利审查标准以及司法实践中强调要遵守专利先申请原则,这是正确的。为了维持专利先申请原则,补交的实验数据通常只能用于佐证原说明书中明确记载或者隐含的技术效果,消除审查员的疑惑,巩固审查员的内心确信,而不能用于引入原说明书中没有的新的技术内容。但是,对专利先申请原则的把握不能过于机械,不能仅因为补交实验数据所证明的技术效果未在原说明书中明确记载,就认定其为新的技术内容而拒绝采纳。只要补交的实验数据所证明的技术效果是本领域技术人员基于专利申请日的知识和能力,根据原说明书公开的内容(包括明确公开和隐含公开的内容)能够明确得到或者推导得出,就应当予以考虑。这样做并不会破坏专利先申请原则。
第二,“公开换保护”原则。专利申请人想保护什么技术方案,就必须先公开该技术方案。未公开的技术内容,不得纳入专利权的保护范围。采纳当事人补交的实验数据,同样不得破坏“公开换保护”的原则。如果专利申请人隐藏一些关键的技术内容,未在说明书中公开,却想获得专利权保护,这就违背了“公开换保护”的原则。基于“公开换保护”原则,只有原说明书中公开披露的技术方案才能纳入专利权的保护范围。在审查当事人补交的实验数据时,同样应当遵守“公开换保护”的原则。凡是原说明书没有公开的内容,不得纳入专利权的保护范围。说明书公开的内容既包括说明书明确记载的内容,也包括说明书隐含公开的内容。因此,只要补交的实验数据所证明的技术效果是原说明书中明确记载或者隐含的,本领域技术人员基于原说明书的记载可以明确知道或者推导得出的,就应当予以考虑。
五、对最高法院征求意见稿的评价和修改建议
最高法院的征求意见稿第13条区分补交的实验数据的不同证明目的,采取了不同的标准,即在适用专利法第26条第3款和第22条第3款时对当事人补交的实验数据采取不同的司法审查标准。
首先,征求意见稿采取双重标准,依据并不十分充分,采取统一的标准更加妥当。无论是判断发明是否符合专利法第26条第3款的规定还是第22条第3款的规定,都必须以原专利申请文件公开或隐含的技术内容为准,这是坚持专利先申请原则的应有之义。补交的实验数据只能用来佐证原专利申请文件所公开或隐含的技术内容,消除审查员的怀疑,巩固审查员的内心确信。因此,对当事人补交的实验数据应当坚持统一的审查标准。
其次,最高法院的本意应当是在适用专利法第26条第3款时对当事人补交的实验数据采取相对严格的审查标准,而在适用专利法第22条第3款时对当事人补交的实验数据采取相对宽松的标准。根据征求意见稿第13条的现有表述,第2款的审查标准比第1款的审查标准还严格,这应当不是最高法院的本意,属于表述上的瑕疵。
再次,征求意见稿确立的标准偏严,不利于创新型医药企业的发展,不利于医药专利的保护,从医药行业的发展出发,应当适当放宽标准。对此,我们可以参考欧洲、美国及日本的审查标准。
最后,作为本文的一个结论性意见,笔者建议最高法院在适用专利法第26条第3款和第22条第3款时,对当事人补交的实验数据采取相同的审查标准——补交的实验数据系采用涉案专利申请日前的实验方法获得的,其所证明的技术效果从原专利申请说明书中可以明确得到或者推导得出。征求意见稿第13条可修改如下:
化学发明专利申请人、专利权人在申请日以后提交实验数据,用于进一步证明发明符合专利法第二十二条第三款和第二十六条第三款的规定的,若该实验数据系采用涉案专利申请日前的实验方法获得,其所证明的技术效果从原专利申请说明书中可以明确得到或者推导得出的,人民法院应当予以审查。